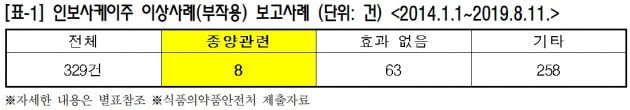
코오롱생명과학의 인보사케이주와 관련해 위암 등 종양 관련 부작용 보고가 8건이 있었던 것으로 나타났다.
4일 국회 보건복지위원회 소속 정춘숙 더불어민주당 의원이 식품의약품안전처로부터 받은 자료에 따르면, 2014년부터 올 8월11일까지 인보사와 관련해 총 329건의 부작용이 보고됐다. 이 가운데 종양 관련 보고는 총 8건으로 종양의 종류는 악성자궁내막신생물, 위암종 2건, 췌장암, 간신생물, 여성악성유방신생물, 악성자궁내막신생물, 이차암종 등이었다.
인보사는 주요 성분이 종양 유발 가능성이 있는 신장세포로 바뀐 사실이 드러나 지난 5월 판매허가가 취소됐다.
'효과 없는 약'이라고 보고한 사례도 총 63건, 19.1%에 달했다. 인보사 이 외의 다른 무릎(슬관절) 주사제의 전체 이상반응 중 효과 없는 약이 차지하는 비중 10.7%와 비교할 때, 2배 가까이 높았다.
정 의원실은 이보다 더 큰 문제는 종양 관련 부작용 사례 8건에 대해 식약처가 역학조사조차 실시하지 않았다는 것이라고 주장했다. 의원실이 종양 관련 부작용 8건에 대한 역학조사 등을 어떻게 실시하고 있는지를 확인한 결과, 식약처는 "종양 관련 이상사례에 대하여는 원보고자의 평가결과 가능성 적음, 평가곤란, 평가불가로 보고돼 현재까지 역학조사는 진행하고 있지 않다"고 답변했다.
의원실에서 왜 역학조사를 실시하지 않고 있느냐 재차 확인하자 식약처는 전체적인 재검증을 지시했다.
정 의원은 "인보사케이주가 현재까지는 허가 시 독성자료와 방사선조사 등을 고려할 때, 큰 우려가 없다는 것이 대부분의 전문가 판단"이라며 "그러나 그럼에도 투여환자 등록 및 15년 간 장기추적조사 등 특별 관리를 실시하는 이유가 종양유발 가능성이 있는 신장세포이기 때문인데, 위암 같은 종양 관련 보고가 접수됐음에도 식약처가 역학조사조차 하지 않다는 것은 문제가 있다"고 했다.
이어 "인보사케이주가 많은 국민들께 투여된 만큼 부작용 보고 시 역학조사 등 식약처의 더욱 적극적인 환자안전관리 대책이 필요하다"고 강조했다.
한민수 한경닷컴 기자 hms@hankyung.com
관련뉴스














