`꿈의 치료제`로 불리는 카티(CAR-T)치료제가 처음으로 국내 병원에서 자체 생산된다.
서울대병원의 `소아청소년 급성림프모구백혈병 대상 CAR-T 치료 임상연구` 승인이 8일 이뤄진 덕택이다.
이는 국내 최초 고위험 첨단재생의료 임상연구 승인이다.
기존 해외 CAR-T 치료제는 비용이 회당 5억 원에 달했지만, 이번 승인에 따라 환자(재발성·불응성 소아청소년 급성림프모구백혈병 환자 대상 예정)들은 병원에서 생산한 CAR-T 치료제를 무상으로 공급받을 수 있다.
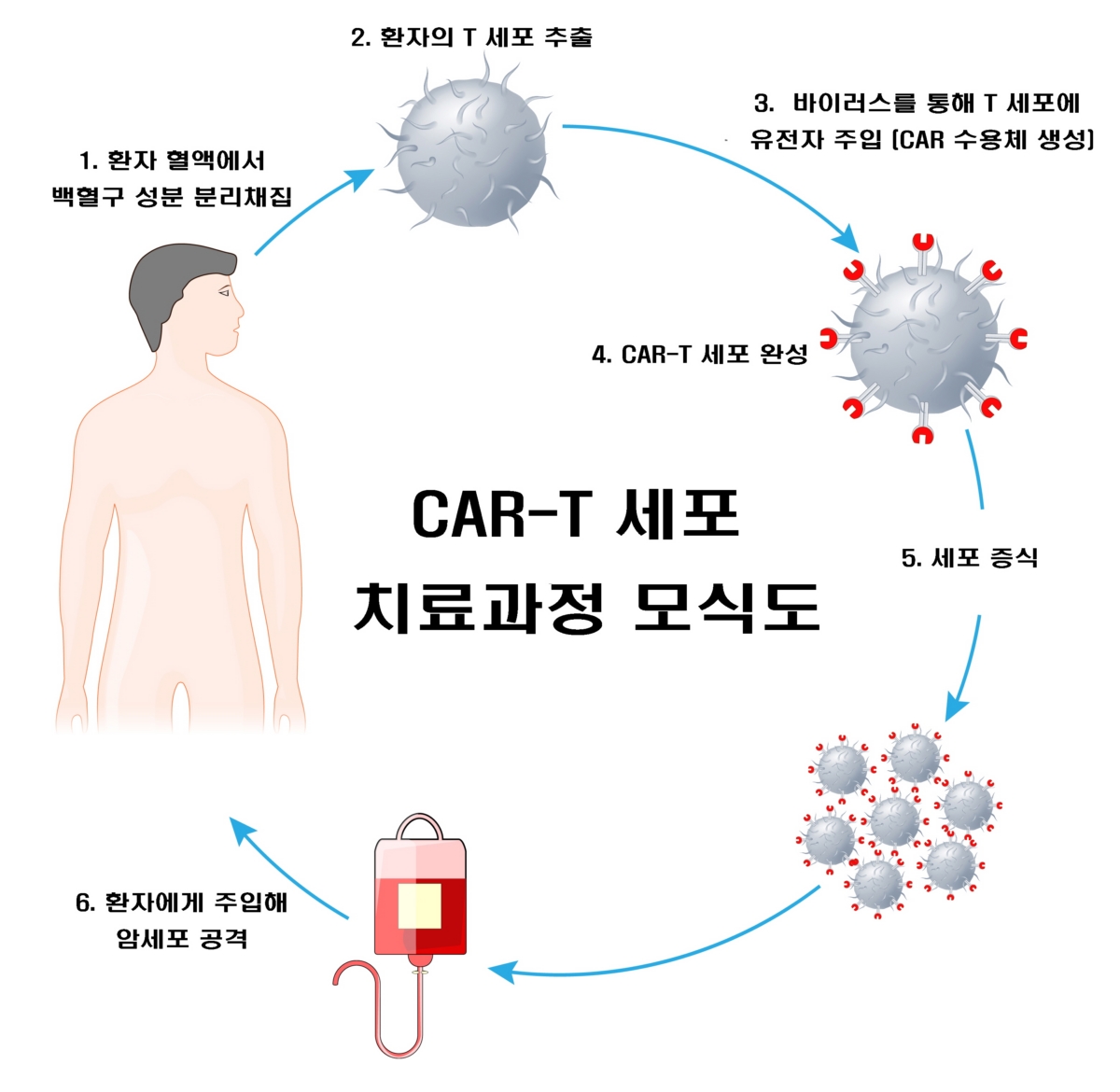
CAR-T 치료는 환자 혈액에서 얻은 면역세포(T세포)가 암을 잘 인식할 수 있도록 유전자 조작을 거친 뒤 배양, 다시 환자의 몸속에 집어넣는 치료법이다.
면역세포가 암세포만을 정확하게 표적하면서도 체내 정상세포 손상을 최소화해 획기적인 최신 치료법으로 주목받고 있다.
병원 자체 생산 치료제기 때문에 비용 뿐 아니라 속도 면에서도 우수하다.
기존 CAR-T 치료제는 환자의 T세포를 해외로 보내고, 증식해 다시 주입하기까지 평균 3주가 소요됐다.
이번 CAR-T는 병원에서 생산되기에 평균 12일로 획기적으로 단축된다.
연구 책임자인 강형진 서울대병원 소아청소년과 교수는 "오랜 심의 끝에 연구계획을 승인받아 기쁘지만 국내 최초의 연구인 만큼 오랜 심의를 거쳤고, 그사이 치료를 받지 못한 환아들에 대한 아쉬움이 남는다"며 "이번 연구가 비용 부담으로 CAR-T 치료를 받지 못한 국내 소아청소년 백혈병 환아들에게 희망이 되기를 기대한다"고 말했다.
서울대병원은 국내 연구자들이 개발한 CAR-T들이 환자들에게 쉽게 적용될 수 있도록 병원 자산을 활용해 GMP생산-전임상시험-임상시험까지 한꺼번에 진행할 수 있는 ‘CAR-T 개발 원스톱 시스템’을 준비 중이다.
또한, 이번 소아백혈병 뿐 아니라 여러 질환에서 CAR-T 치료제 개발을 위해 노력할 예정이라고 밝혔다.
관련뉴스















