(서울=연합뉴스) 서한기 기자 = 식품의약품안전처는 최소한의 안전성이 검증된 임상시험용의약품 가운데 치료목적으로 사용할 수 있게 승인한 건수가 올해 들어 7월까지 398건으로 집계됐다고 29일 밝혔다.
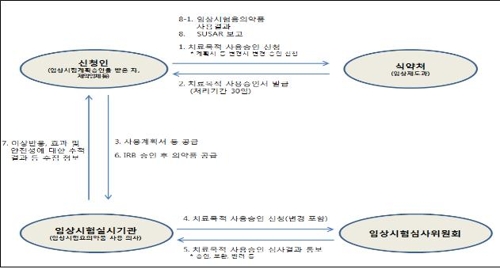
식약처는 2002년부터 '임상시험용의약품의 치료목적 사용승인' 제도를 시행하고 있다. 생명을 위협하는 질환이 있는 환자가 다른 대체치료 수단이 없으면 원칙적으로 임상시험용으로만 사용할 수 있는 의약품을 품목허가를 받기 전에 예외적으로 사용할 수 있도록 승인하는 제도를 말한다.
미국과 유럽 등에서도 우리나라와 동일하게 해당 국가에서 '임상시험' 승인을 받은 의약품에 한해 치료목적으로 사용할 수 있게 하고 있다.
이런 '치료목적 사용승인 제도 시행 이후 올해 7월까지 승인된 건수는 4천842건에 달했다.
질환별로는 폐암 등 호흡기질환(202건)이 가장 많았고, 위암 등 소화기질환(110건), 유방암 등 여성질환(39건), 악성흑색종 등 피부질환(21건), 백혈병 등 혈액질환(10건), 기타 질환(16건) 등의 순이었다.
한편, 국내 개발 중인 방사성의약품(루테슘, Lu177)의 경우 보건복지부의 예산지원을 받아 동물실험 등 연구진행 중이며, 임상시험 승인을 받지 않아 최소한의 안전성이 검증되지 않은 물질로서 '치료목적 사용승인' 대상이 될 수 없다고 식약처는 설명했다.

shg@yna.co.kr
(끝)
<저작권자(c) 연합뉴스, 무단 전재-재배포 금지>
관련뉴스













