 과학기술정보통신부 산하 한국연구재단은 성균관대 김경규 의학과 교수·이정헌 신소재공학부 교수, 유상렬 서울대 식품공학과 공동 연구팀이 ‘활성산소’로 내성균을 골라 죽이는 나노미터(㎚·1㎚=10억분의 1m) 크기의 로봇을 개발했다고 최근 밝혔다.
과학기술정보통신부 산하 한국연구재단은 성균관대 김경규 의학과 교수·이정헌 신소재공학부 교수, 유상렬 서울대 식품공학과 공동 연구팀이 ‘활성산소’로 내성균을 골라 죽이는 나노미터(㎚·1㎚=10억분의 1m) 크기의 로봇을 개발했다고 최근 밝혔다.항생제는 세균 내 단백질을 표적으로 한다. 항생제에 노출된 세균은 스스로 돌연변이를 일으켜 표적이 된 단백질 구조를 바꾼다. 그래서 세균의 세포막을 깨뜨려 죽이는 방식의 항생제가 개발됐지만, 이 역시 내성균 발생을 막진 못했다.
김경규 교수는 “내성균 문제는 감염질환 치료를 항생제 개발 이전 상태로 되돌릴 수도 있는 매우 심각한 문제”라고 설명했다. 이어 “현재 항생제로는 해결할 수 없기 때문에 완전히 다른 방식으로 작동하는 항생제를 개발할 필요가 있다”고 덧붙였다.
연구팀은 화학적 방식이 아니라 물리적 힘으로 세균 세포막을 깨면 내성이 발생하지 않을 것이라고 가정했다. 그래서 고안한 게 항생제 역할을 하는 나노로봇, 이른바 ‘항생나노봇’이다.
먼저 산화철 나노입자에 단백질 ‘엔도라이신’을 코팅했다. 엔도라이신은 박테리오파지(세균을 먹어치우는 바이러스)가 세균에 몰래 기생할 때 쓰는 수단이다. 우주선이 국제우주정거장에 도킹하듯 박테리오파지가 세균에 안착할 수 있어 ‘도킹 단백질’로도 불린다. 균이 있는 곳을 감지해 달려가 결합할 수 있는 로봇 근육(액추에이터)과 센서를 만든 것이다.
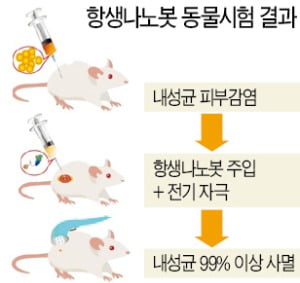
연구팀은 황색포도상구균 내성균을 쥐에 감염시킨 뒤 항생나노봇을 넣고 전기 신호를 가했다. 그때 산화철 나노입자에서 활성산소가 뿜어져나와 세균 세포막을 효과적으로 파괴하는 것을 현미경으로 확인했다.
연구팀 관계자는 “내성균이 99% 이상 사멸됐다”고 말했다. 이어 “철 나노입자를 실리콘 및 단백질로 코팅했고, 피부 미용에 사용되는 낮은 전기자극으로 항생나노봇을 구동할 수 있도록 했다”며 임상 적용 가능성이 높다고 설명했다. 나노로봇은 인체에 미칠 영향을 가늠하기 쉽지 않아 임상에 진입하려면 생체 적합성 등 여러 단계의 검증이 필요하다. 이번 연구 결과는 나노의학 분야 국제학술지 ‘스몰’에 실렸다.
박종오 전남대 교수가 이끄는 한국마이크로의료로봇연구원은 고형암 진단과 치료가 가능한 직경 100㎚ 크기 의료용 나노로봇을 개발 중이다. 암을 찾아가는 표적 물질로 엽산을 썼다. 왕성하게 영양분을 먹어치우는 암세포 대부분 표면에 엽산 수용기가 많다는 점에 착안한 것이다. 그리고 근적외선을 쪼였을 때 열과 약물을 함께 방출하도록 금 입자와 자성 나노입자, 폴리도파민과 항생제를 넣었다.
아직 동물시험 단계로 쥐와 토끼를 대상으로 연구하고 있다. 공동 연구 중인 김규표 서울아산병원 종양내과 교수는 “아직 개념 증명 단계지만 이 기술이 실현되면 암 조직으로의 약물 전달을 극대화하면서 주변 정상 조직이 입는 피해를 최소화할 수 있게 된다”고 설명했다.
이해성 기자
관련뉴스














