
많은 국내외 기업이 알츠하이머병 신약 개발을 위해 자웅을 겨루고 있다. 경쟁에서 살아남으려면 고유한 타깃과 인지 개선에 대한 명확한 효능, 두 가지 무기를 갖춰야만 한다. 셀리버리는 이 두 조건을 모두 갖췄다고 평가받는 기업이다.
파킨 단백질, 독성 단백질과 고장 난 미토콘드리아 한 방에 정리
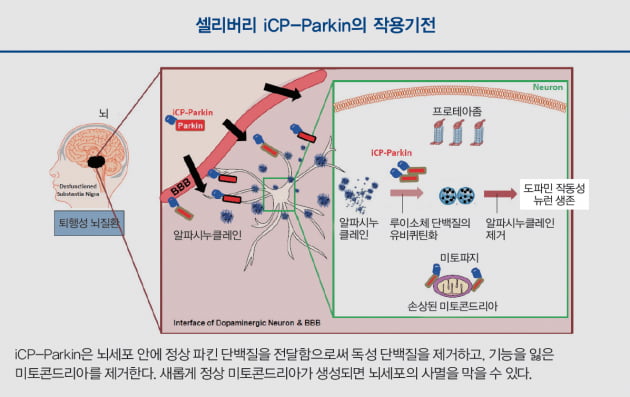
셀리버리의 첫 번째 무기는 ‘파킨(Parkin) 단백질’이다. 파킨슨병과 이름이 유사해 오해하기 쉽지만, 파킨은 E3 리가아제 중 하나다. E3 리가아제는 세포 내의 잘못된 단백질을 제거하는 여러 기작 중 하나인 ‘유비퀴틴-프로테아좀(UPS)’에 관여하는 효소다. 즉 파킨은 뇌세포에서 발생하는 여러 독성 단백질을 제거하는 데 활용될 수 있다는 의미다.
뇌세포의 아밀로이드 베타 단백질은 단량체로 존재할 때는 큰 문제가 없지만, 이들이 엉겨붙어 올리고머, 그리고 플라크가 되면 독성을 나타내기 시작한다. 파킨슨의 원인으로 알려진 알파시누클레인 단백질 역시 마찬가지다. 독성 단백질이 쌓이면 파킨과 같은 단백질 효소들도 영향을 받는다. E3 리가아제들의 기능이 떨어지면 독성 단백질을 제거하지 못하고, 이들은 다시 E3 리가아제의 기능을 더 망가뜨리는 악순환이 반복된다.
망가지는 건 효소만이 아니다. 세포에서 에너지를 생산하는 역할을 맡고 있는 미토콘드리아가 직격탄을 맞는다. 미토콘드리아가 손상되면 세포의 모든 기능이 저하되기 때문에 뇌세포 사멸로 이어진다. 뇌세포의 사멸을 막기 위해서는 손상된 미토콘드리아를 제거하고, 정상 미토콘드리아가 만들어져야 한다.
셀리버리는 이 악순환의 고리를 끊어내는 것이 파킨 단백질이라고 판단했다. 조대웅 셀리버리 대표는 “정상적인 파킨 단백질을 뇌세포로 주입할 수만 있다면 인지 개선이 가능할 것이라고 봤다”고 말했다.
TSDT 플랫폼, BBB 혈관세포 통과해 뇌 안으로 진입
문제는 파킨 단백질이 매우 크다는 점이었다. 뇌혈관장벽(BBB)은 500달톤 이하의 저분자 약물만이 통과가 가능한 것으로 알려져 있다. 파킨 단백질은 6만7000달톤으로 매우 큰 물질이다. 셀리버리는 두 번째 무기, TSDT 플랫폼을 이용해 이 문제를 해결했다.
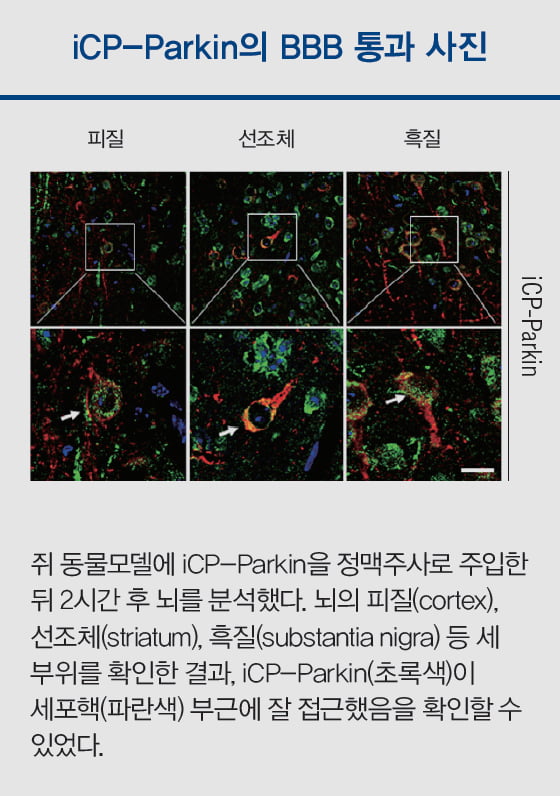
TSDT는 크게 약물과 세포 투과성 펩타이드인 CPP(hydrophobic Cell-Penetrating Peptide)로 구성돼 있다. CPP는 V 자 모양의 소수성 펩타이드로 세포막에 일종의 구멍을 뚫는 역할을 한다. CPP가 열어놓은 구멍으로 거대 약물이 세포 내부로 진입할 수 있다. 즉 BBB를 구성하는 혈관세포를 통과해 뇌 안쪽으로 진입하겠다는 전략이다. 동물실험 결과 iCP-Parkin이 BBB를 통과해 2시간 이내에 뇌조직에 전송된다는 사실을 확인했다.
혹시 표적세포가 아니라 다른 세포에 들어가는 이른바 ‘오프타깃 효과’가 나타날 위험은 없을까. 조 대표는 “정상세포에 들어가게 되면 그대로 통과하고 손상된 세포에서만 오래 머무르며 약리작용을 한다”고 말했다.
이것이 가능한 이유는 CPP가 세포 안으로 통과하는 것은 물론 세포 밖으로 빠져나가는 데에도 능하기 때문이다. 세포를 들어가고 나가는 데 별도의 에너지가 필요하지 않기 때문에 세포 간 이동이 자유롭다. 조 대표는 “정상세포에 머무는 시간은 짧지만 만약 오래 머물게 되더라도, 할 일이 없는 파킨 단백질이 많아지면 세포는 항상성 유지를 위해 유비퀴틴 기작으로 분해시킨다”고 설명했다.
실제 지난해 파킨슨병 동물모델에서 iCP-Parkin의 효과와 안전성을 확인했다. 병증이 나타난 동물모델에 iCP-Parkin을 주입하자 운동 기능을 90%가량 회복했고, 파킨슨병환자에게서 나타나는 알파시누클레인 단백질의 91%가 제거되는 것을 확인했다. 이 결과는 국제학술지 <사이언스 어드밴시스>에 게재되기도 했다.
기술이전, 빠르면 올해 안에 승부 날 것
지난 3월 iCP-Parkin의 대량생산에 성공하면서 현재 비임상을 준비하고 있다. 그간 iCP-Parkin의 대량생산이 상용화의 큰 허들 중 하나로 지적됐던 셀리버리로서는 한숨 돌린 셈이다.
iCP-Parkin은 CPP와 약리물질이 링커로 연결된 형태가 아니라 하나로 합쳐진 복합체다. 세포를 통과할 때 두 물질이 분리될 걱정은 없지만, 약물을 균일한 품질로 대량생산하기가 어렵다.
조 대표는 “약물의 구조와 생산공정을 여러 차례 바꿔가며 결국 최적의 조합을 찾아냈다”며 “우리가 개발한 공정기술을 미국의 위탁생산(CMO) 업체인 KBI에게 전달해 임상에 사용될 약물을 생산하고 있다”고 말했다.
이후 시료 생산이 완료되면 미국의 임상시험수탁기관(CRO)인 아투카를 통해 파킨슨병의 비임상부터 진행할 예정이다. 임상을 모두 미국에서 진행해 향후 미국 식품의약국(FDA)의 치료 목적 사용 승인으로 상용화를 앞당기겠다는 전략이다.
조 대표는 “iCP-Parkin의 기술이전 역시 진행 중에 있다”며 “글로벌 톱티어 기업들과 기술검증을 하고 있는 단계로 빠르면 올해 안에 승부가 날 것”이라고 말했다.
◎전문가 평가
<i>iCP-Parkin 동물실험 결과 국제학술지 게재, 기술이전 협상 기대
by 안병규 에이스톤벤처스 부사장 </i>
TSTD 플랫폼을 활용한 iCP-Parkin은 지난해 캐나다와 한국에서 특허등록을 완료했다. 4월 <사이언스 어드밴시스>에 게재된 논문에서도 손상된 미토콘드리아의 기능이 회복되는 등의 효능을 확인해, 미국·일본 등의 빅파마와 기술이전을 진행할 것으로 기대된다.
최지원 기자
*이 기사는 <한경바이오인사이트> 매거진 2021년 6월호에 실렸습니다.
관련뉴스














