엔지켐생명과학이 코로나19 폐렴 환자를 대상으로 진행한 'EC-18'의 국내 임상 2상에서 1차 평가지표의 통계적 유의성을 확인하지 못했다. 2차 평가지표를 충족한 만큼 임상 설계를 변경해 후속 임상을 진행한다는 계획이다.
엔지켐생명과학은 EC-18 임상 2상에서 2차 평가지표인 회복기간 및 사이토카인 폭풍 억제와 관련한 유의미한 결과를 얻었다고 30일 밝혔다. 회사는 임상 2상 결과를 근거로 대상자 회복기간(Time to recovery)을 주평가지표로 변경해 코로나19 환자 대상 임상 2b상 혹은 3상을 진행할 예정이다.
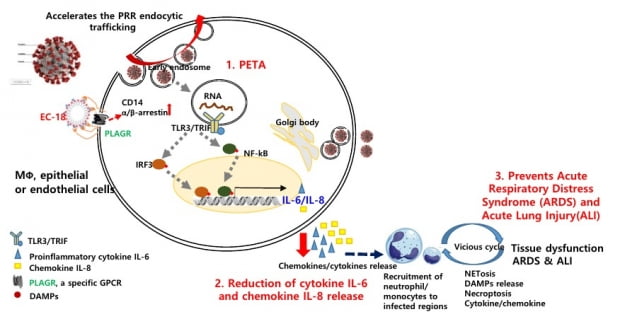
EC-18은 엔지켐생명과학이 패턴인식수용체 세포 내 재순환 촉진(PETA) 기전을 바탕으로 개발 중인 신약후보물질이다. 작년 5월 국내에서 두 번째로 코로나19 치료제 임상 2상을 승인받았다.
임상 2상의 1차 평가지표는 ‘1회 이상 투여한 경증 폐렴 환자에서 14일 이내에 산소 치료가 필요한 중증 폐렴 또는 급성호흡곤란증후군(ARDS)으로 이행되는 확률’이었다.
엔지켐생명과학은 지난 27일 1차 평가지표에 대한 통계적 유의성을 확인하지 못했다고 공시했다. 임상 대상자의 수가 적고, 이상 반응 발생 시 투약을 즉시 중단하도록 설계돼 유효성을 제대로 평가할 수 없었다는 설명이다. 총 14일간 1일 1회 경구 투약하며 유효성을 평가하려 했지만, 증상 악화 또는 이상반응으로 중도 탈락으로 투약이 중단되는 제약이 있었다는 것이다.
2차 평가지표에서는 EC-18이 염증성 사이토카인인 ‘인터루킨6(IL6)’ 및 'IL8'을 감소시키는 것을 확인했다. IL-8은 투여 후 1일차에 비해 14일차에 유의미하게 줄었다(p=0.0032). IL-6은 50~64세 연령군에서 시험 1일차에 비해 시험 14일차에 통계적으로 유의한 수준으로 감소(p=0.0021)했다.
임상 대상자의 증상 호전 정도를 보여주는 지표인 영국조기경고점수(NEWS)도 확인했다. 그 결과, 50~64세 연령군에서 투약 전 대비 투약 8~14일까지 EC-18 투약군의 평균 NEWS 값은 위약군보다 통계적으로 유의미하게 감소했다.
엔지켐생명과학 관계자는 “여러 선행 연구들과 일관되게 EC-18의 핵심 작용 기전인 면역조절 효과를 코로나19 폐렴 환자에서도 확인했다”고 말했다.
EC-18 투약군 및 위약군의 비교 결과, 안전성 측면에서도 통계적인 차이가 관찰되지 않았다. 대부분의 이상 반응은 경증이었으며 활력징후 및 심전도 등에서도 임상적으로 유의미한 이상 반응은 관찰되지 않았다.
박인혁 기자
관련뉴스














