시오노기제약은 S-217622 임상 2·3상을 2a상과 2b·3상으로 나눠 진행 중이다. 이 중 2a상은 증상이 없거나 경미한 코로나19 환자를 대상으로 실시했다. 무작위배정, 위약 대조, 이중 눈가림(맹검) 방식이었다. 약을 5일간 1일 1회 경구 투여해 항바이러스 효과와 안전성을 평가했다.
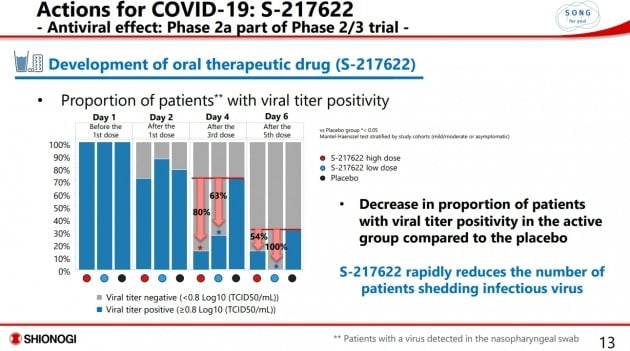
시오노기제약에 따르면, S-217622 복용군의 바이러스 역가(양)가 위약군 대비 더 많이 줄었다. 4일째 위약군의 바이러스 역가가 약 30% 감소한 데 비해 S-217622 고용량 복용군에서는 80%, 저용량군에서는 63% 감소했다. 바이러스 감소 속도 역시 S-217622 복용군이 위약군보다 더 빨랐다. 중대한 이상 반응이 관찰되지 않아 안전성도 확인했다는 설명이다.
회사 측은 “이번 2a상을 포함해 임상이 진행되는대로 결과를 일본 의약품및의료기기관리청(PMDA)에 순차적으로 제출하고 있다”고 했다. 앞서 진행한 비임상 및 임상 1상 결과도 PMDA에 제시했다고 했다.
S-217622는 일본 홋카이도대와 시오노기가 공동 개발한 '3CL' 단백분해효소 억제제다. 코로나 바이러스(SARS-CoV-2)에는 바이러스 복제에 필수적인 3CL 프로테아제라는 효소가 있다. S-217622는 이 3CL 프로테아제를 억제해 바이러스 복제를 막는다.
시오노기제약에 따르면 비임상에서 S-217622는 알파 베타 감마 델타 변이에서 모두 유사한 수준의 바이러스 증식 억제 능력을 갖는 것이 확인됐다. 지난해 12월 오미크론 변이를 대상으로 한 체외실험(in vitro)에서도 바이러스 증식 억제효과를 보였다고 했다.
S-217622는 화이자의 ‘팍스로비드’와도 비교된다. 두 약 모두 3CL 프로테아제를 표적하기 때문이다. 시오노기제약은 팍스로비드 대비 적은 복용량을 강점으로 내세우고 있다. 또 복용 대상에 팍스로비드에는 없는 무증상자를 넣어 대상군을 넓혔다.
S-217622는 현재 일본 뿐 아니라 한국 싱가포르 베트남 유럽 등 14개국에서 임상을 진행 중이거나 준비 중이다. 글로벌 임상의 전체 규모는 약 2000명이다.
국내에서는 일동제약이 S-217622의 임상 2·3상을 진행 중이다. 일동제약은 지난해 말 시오노기와 협약을 맺고 한국 내 임상을 주도하고 있다.
최근 2b·3상 참여자 모집에 들어갔다. 내달 중순까지 2b·3상을 마치겠다는 계획이다. 이후 4월 중순에는 식품의약품안전처로부터 긴급사용승인을 받을 수 있을 것으로 기대하고 있다.
이도희 기자
관련뉴스














