메드팩토의 주가는 지난 4~5일 이틀간 26.4% 하락했다. 경쟁 약물을 개발하는 미국 아게누스가 긍정적인 임상 1b상 결과를 발표해서다. 아게누스는 최근 유럽종양학회 주관 위장관조양학회(ESMO GI)에서 대장암(MSS-CRC) 대상 항 CTLA-4 항체인 ‘보텐실리맙’과 항 PD-1인 ‘발스틸리맙’ 병용 1b상 결과를 발표했다. 객관적반응률(ORR) 23%, 전체생존기간 중간값(mOS) 20.9개월이었다.
메드팩토는 주요 후보물질인 ‘백토서팁’과 키트루다의 병용으로 MSS-CRC 대상 1b·2a상에서 300mg 투약(BID) 기준 ORR 18.2%, mOS 17.3개월을 확인했다. 메드팩토는 글로벌 임상 1b·2a상을 통해 타 임상 및 표준 치료 요법(Standard of Care) 대비 우월한 데이터를 확인하고, 현재 미국 식품의약국(FDA) 2b·3상을 준비하고 있다.
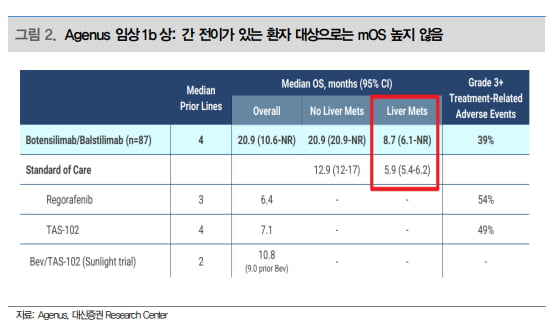
이번에 아게누스가 발표한 데이터는 메드팩토의 1b·2a상 대비 우월한 임상 결과다. 다만 아게누스 임상은 간 전이가 없는 환자를 대상으로 진행한 결과임에 주목해야 한다고 했다. 이에 메드팩토 임상과 직접적인 비교는 어렵다는 판단이다.
한송협 연구원은 “백토서팁과 키트루다 병용은 대부분 간 전이가 있으면서 2차 치료를 마친 예후가 좋지 않은 환자를 대상으로 진행한다”며 “아게누스 임상에서 간 전이가 있는 환자들의 경우 mOS는 8.7개월에 불과하다”고 설명했다.
현재 표준 치료요법인 ‘레고라페닙’을 간 전이가 없는 환자를 대상으로 분석한 데이터에서는 ORR은 36.4%, mOS가 22개월이다. 실제로 아게누스의 주가는 이번 발표 이후 큰 변동이 없었다고 했다.
한 연구원은 “이번 메드팩토 주가 하락은 경쟁사의 임상 결과 발표가 메드팩토의 파이프라인 가치를 저해하는 이벤트가 아니라는 점에서 시장의 오해에 따른 것“으로 판단했다.
또 “FDA 임상 3상 승인 일정이 확실하게 제시되지 않는 점 또한 불안감을 증폭시키는 요인”이라며 “하지만 해당 임상은 글로벌 협력사의 일정에 맞춰 진행하기 때문에 타임라인 공개에 어려움이 있다”고 설명했다.
메드팩토의 올 1분기 기준 현금성 자산은 200억원 수준으로, 자금조달이 당장 필요한 상황은 아니라고 했다.
김예나 기자 yena@hankyung.com
관련뉴스














