
제약업계의 투자심리 위축이 장기화되면서 국내 신약벤처기업의 후보물질 임상개발 중단 소식이 잇따르고 있다. 운영자금과 임상 비용을 줄이기 위한 목적으로 ‘허리띠 졸라매기’에 들어갔다는 분석이 나온다. 국내외 신약개발 속도도 과거에 비해 빨라지면서 시장 환경이 바뀌거나 속도 경쟁에서 밀려 연구개발이 중단되는 사례도 늘어나고 있다.
○급박한 시장 변화로 임상 중단
19일 한국거래소에 따르면 지난 달(9월 1일~9월 31일) 중 임상개발 중단을 공시한 코스닥 바이오기업은 브릿지바이오테라퓨틱스 외 6곳이었다. 11개 임상개발 프로그램이 중단됐다. 수시 공시 대상에 들어가지 않는 전임상 단계 물질 개발을 중단한 사례나, 공시 의무가 없는 비상장기업의 사례까지 더하면 ‘후보물질 다이어트’의 사례는 이보다 더 많을 것으로 추산된다.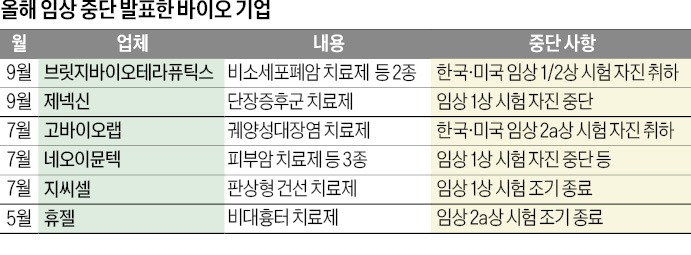
이중에서도 브릿지바이오의 비소세포폐암 표적항암제 후보물질(BBT-176) 임상개발 중단은 이례적인 사례로 꼽힌다. 지난 달 싱가포르에서 열린 국제학회에서 구두발표를 통해 임상 1상 결과를 알렸던 ‘간판 후보물질’의 연구개발이 돌연 중단된 것이다.
이정규 브릿지바이오 대표는 “2017년 한국화학연구원으로부터 물질을 도입해 개발해오면서 그간 유사한 약물의 임상개발이 국내외에서 10개로 늘어났다”며 “신약으로서의 성공 가능성이 불투명하다고 보고 개발 중단을 결정했다”고 밝혔다. 바통은 이제 갓 임상에 진입한 BBT-207이 넘겨받는다.
이 대표는 “개발 속도는 늦지만 BBT-207이 더 우수한 효능이 예상돼 신약으로서 가능성이 더 높다고 봤다”고 설명했다. 업계에서는 브릿지바이오의 현금 상황도 영향을 미쳤을 것으로 보고 있다. 개발 자금이 풍부하다면 BBT-176과 BBT-207을 순차적으로 개발하면 되지만 그렇지 않다보니 ‘선택과 집중’을 할 수밖에 없었다는 얘기다.
고바이오랩 또한 후속 후보물질의 비임상 결과가 더 우수해 임상 1상까지 마친 궤양성 대장염 연구 중단을 지난 7월 발표했다. 고바이오랩 관계자는 “임상개발 중단을 결정한 것은 기대한 결과가 나오지 않으면 수십억 원 이상의 손해를 보기 때문”이라며 “매몰비용을 잃고, 당장 주가에도 부담이 될 수 있어도 향후 사업성과 보장이 어렵다는 판단이 서면 접는 것이 합리적인 판단”이라고 말했다.
○ 제동걸린 ‘원소스 멀티유즈’
개발 중인 신약의 쓰임새를 넓히기 위해 여러 질환을 대상으로 동시 진행하던 임상시험도 중단되는 사례가 줄줄이 나오고 있다.자금 사정이 좋을 땐 개발 약물의 시장성도 높일 수 있고, 다양한 질환에서 가능성을 모색할 수 있다는 장점이 있지만 그렇지 않을 땐 임상 비용이 커지는 문제가 있다. 주로 1개 후보물질로 여러 임상을 수행하던 업체들이 이런 방식으로 다이어트를 위한 ‘칼’을 빼들었다.
네오이뮨텍은 10종류의 암을 대상으로 면역항암제 후보물질인 ‘NT-I7’로의 임상을 진행하던 중 지난 7월 피부암, 위암 등 3개 암에 대한 임상 중단을 발표했다. 췌장암과 대장암 등 미충족수요가 큰 암으로 역량을 집중한다는 계획이다.
○임상 환자 못모아 연구개발 중단
임상에 참여할 환자를 구하지 못하는 것도 임상 중단이 중단되는 주요 사유로 꼽힌다. 진원생명과학은 미국에서 진행하던 코로나19 스프레이 치료제의 임상 2상을 조기 종료했다.진원생명과학 관계자는 “코로나19에 감염되지 않은 의료인 225명을 모집하려고 했지만 4분의 3 수준 밖에 모이지 않아 중단하게 됐다”며 “감염병 연구는 유행 상황과 백신 개발 등 환경 변화의 영향을 많이 받는다”고 말했다.
지난 9월 제넥신도 희귀질환인 단장증후군 환자 모집에 어려움을 이유로 신약후보 ‘GX-G8’의 임상 1상을 자진 중단한다고 발표했다.
이우상/이영애 기자 idol@hankyung.com
관련뉴스














