한미약품이 최근 미국 식품의약국(FDA)에 차세대 비만 치료 삼중작용제(HM15275) 임상 1상 진입을 위한 임상시험계획(IND)을 신청했다고 1일 발표했다.
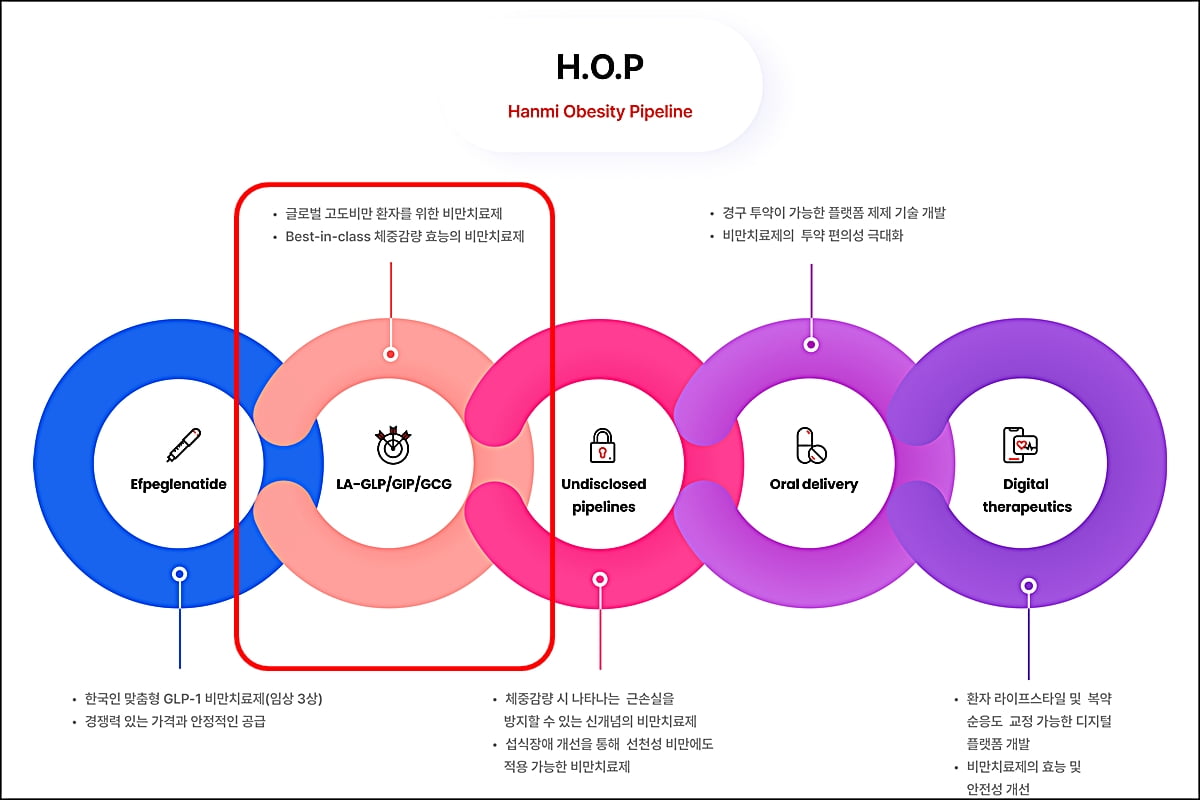
한미약품은 HM15275의 상용화 목표 시점을 2030년으로 정하고 지난 2월 29일 한국 식품의약품안전처에 IND를 제출했다. HM15275는 현재 임상 3상시험을 진행하고 있는 에페글레나타이드의 후속 비만 신약이다.
글루카곤 유사 펩타이드(GLP-1)와 위 억제 펩타이드(GIP), 글루카곤(GCG) 등의 수용체 작용을 최적화해 근 손실을 최소화하면서도 25% 이상의 체중 감량 효과가 기대된다. 한미약품은 오는 6월 미국에서 열리는 2024 미국당뇨병학회(ADA)에서 HM15275에 대한 임상 연구 결과를 발표할 계획이다.
이번 학회에서 한미약품은 HM15275의 계열 내 최고신약 잠재력과 작용 기전 등을 규명한 결과를 공개한다. 비만이 주요 원인이라고 알려진 다양한 심혈관계 질환 모델에서 HM15275의 차별화된 치료 효능을 입증한 결과도 발표한다.
이지현 기자 bluesky@hankyung.com
관련뉴스














