박테리오파지 캡시드에 포도당 입혀 바이러스 결합 유인
독일 '연구그룹 베를린' 협회, 저널 '네이처 나노테크놀러지'에 논문
(서울=연합뉴스) 한기천 기자 = 약칭 '플루(flu)'로 통하는 인플루엔자(독감) 바이러스는 여전히 인류의 건강을 심각하게 위협하는 존재다.
세계보건기구(WHO)에 따르면 해마다 전 세계에서 약 65만명이 이 바이러스 감염으로 목숨을 잃는다.
요즘 의료 현장에서 쓰이는 항바이러스제는 폐 세포에 감염된 이후의 플루 바이러스만 공격해 치료 효과가 제한적이다.
플루 바이러스의 폐 세포 감염을 먼저 차단하면 훨씬 더 효과적일 테지만, 과학자들은 여태껏 그 방법을 알지 못했다.
마침내 독일 과학자들이 플루 바이러스의 폐 세포 감염을 사전 차단하는 획기적인 치료법을 개발했다.
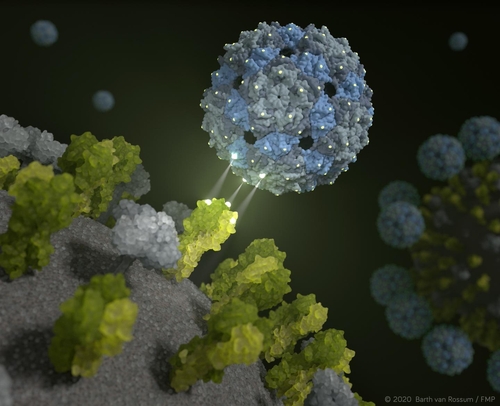
화학적으로 처리된 박테리오파지(세균 먹는 바이러스)의 캡시드(단백질 껍질)로 플루 바이러스를 포박해, 폐 세포 감염과 증식을 억제하는 것이다.
과학자들은 플루 바이러스와 조류 인플루엔자 바이러스에 대한 전 임상 시험에서 효과를 확인한 데 이어 신종 코로나바이러스에 대해서도 이 치료법을 시험할 계획이다.
이 연구 결과를 담은 논문은 저널 '네이처 나노테크놀러지(Nature Nanotechnology)'에 실렸고, 별도의 논문 개요는 30일(현지시간) 온라인(www.eurekalert.org)에 공개됐다.
이 연구는 '연구 그룹 베를린(FVB)' 협회의 주도로, 라이프니츠 분자 약물학 연구소((FMP), 베를린 자유대, 베를린 공대(TU), 훔볼트대(HU), 로버트 코흐 연구소(RKI), 베를린 샤리테 의대 등이 공동 수행했다.
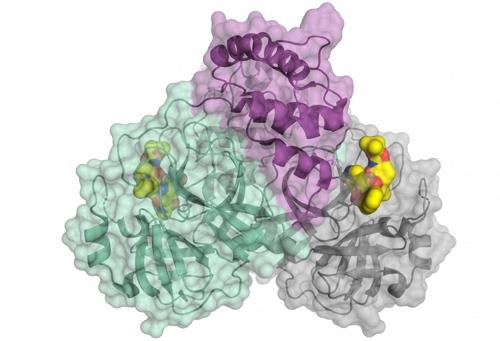
연구팀이 실험에 활용한 건, 장에 서식하는 Q-beta 박테리오파지(약칭 파지)다.
이 파지는, 포도당 분자를 리간드(수용체 결합 분자)로 처리하면, 플루 바이러스 표면의 3원자가 수용체(trivalent receptor)와 잘 들어맞는 표면 특성을 가졌다고 한다.
바이러스 표면에는 예외 없이 3원자가 헤마글루티닌 수용체가 있다. 바이러스의 감염은, 이 수용체가 숙주의 폐 조직 세포 표면에 존재하는 포도당 분자(시알산)와 결합하면서 이뤄진다.
연구팀이 만든 구형의 파지 캡시드는, 껍질만 있는 유사 바이러스 입자로서 일종의 미끼 역할을 한다.
HU의 분자 생체물리학 그룹에서 연구에 참여한 다니엘 라우스터 박사후연구원은 "이 파지 캡시드는, 바이러스 표면의 3가 헤마글루티닌 수용체에 간격을 맞춰 결합하는 180종의 단백질로 구성돼 있다"라면서 "이상적인 바이러스 유인 조건을 갖춘 캡시드를 이용해 바이러스를 무력화하는 것"이라고 설명했다.
Q-beta 파지의 구형 캡시드가 이런 기능을 하기 위해선 화학적 조작이 필요한데, 연구팀은 합성화학 기술로 캡시드의 정해진 위치에 포도당 분자를 붙였다.
연구팀은 동물 모델과 배양세포 실험에서, 이 파지 캡시드가 플루 바이러스에 대해 강한 결합력과 억제력을 모두 갖췄다는 걸 확인했다.
플루 바이러스에 감염된 인간의 폐 조직 세포에 이 파지 캡시드를 투여하면 바이러스는 증식을 멈췄다.
연구팀은 생분해성과 비독성, 비면역성 등이 확인된 파지 캡시드 치료법을, 다른 종의 바이러스와 세균, 특히 신종 코로나바이러스에도 적용할 수 있을 거로 기대한다.
예컨대 신종 코로나바이러스가 숙주의 목이나 기도 세포에 침투하지 못하게 차단하는 치료제를, 같은 원리로 개발할 수 있다는 게 연구팀의 구상이다.
FMP의 화학 생물학과장인 크리스티안 하켄베르거 교수는 "혁신적인 항바이러스제 개발을 위해 완전히 새로운 통찰을 제시한 성공적인 연구 결과"라고 자평했다.
cheon@yna.co.kr
(끝)
<저작권자(c) 연합뉴스, 무단 전재-재배포 금지>
관련뉴스














