식약처, 제약사 '시판 후 조사' 수행을 위한 자료 제공 절차 마련
(서울=연합뉴스) 조현영 기자 = 식품의약품안전처는 코로나19 백신을 만든 제약사가 시판 후 조사에서 실제 병·의원으로부터 수집한 환자 정보인 '실제사용자료'를 이용할 수 있도록 절차를 마련했다고 15일 밝혔다.
시판 후 조사는 시장에 판매 중인 신약을 관찰해 의약품 허가 과정에서 나타나지 않았던 새로운 이상 사례 등 안전성·유효성에 영향을 미치는 요인이 있는지 조사하는 것을 말한다.
그간 코로나19 백신도 다른 의약품처럼 판매 전 조사 계획을 수립해 조사대상자를 등록하고 정보를 수집하는 방식으로 시판 후 조사를 해야 했다.
그러나 팬데믹 상황에서는 조사 계획 수립에 시간이 걸리고 대상자 수가 변동될 수 있어 이 같은 방식으로 조사하기 어렵다는 지적이 있었다.
이에 식약처는 지난 8월 '식의약 규제혁신 100대 과제'에 이 제도 개선을 약속했다.
식약처는 "코로나19 백신은 대규모 집단을 대상으로 짧은 기간 접종이 이뤄져 안전성·효과성에 대한 정보가 많아 실제사용자료를 활용한 시판 후 조사가 가능하다"면서 "질병관리청, 건강보험공단과 협의해 코로나19 백신 시판 후 가명처리된 정보인 데이터베이스 이용 절차를 마련했다"고 밝혔다.
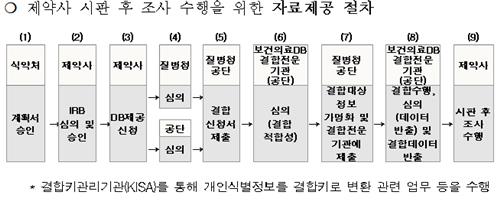
식약처가 제약사가 제출한 시판 후 데이터베이스 연구 계획서를 검토·승인하면 제약사는 질병청과 공단에 데이터 활용 신청서를 발송한다. 질병청과 공단이 이를 검토해 데이터 반출 여부를 결정하면 제약사는 받은 데이터로 시판 후 조사를 수행할 수 있다.
식약처는 이 절차에 대한 안내서를 발간했다며 코로나19 백신 시판 후 조사에 실제사용자료가 원활하게 활용되길 기대한다고 덧붙였다.

hyun0@yna.co.kr
(끝)
<저작권자(c) 연합뉴스, 무단 전재-재배포 금지>
관련뉴스














