美 임상 책임자 "환자 26명에게서 관절 통증, 기능 개선 효과 있었다"
이달 식약처 조건부 허가 받고 시판할 계획이었으나 연내 어려울 듯

네이처셀은 지난 18일 서울 웨스틴조선호텔에서 퇴행성 관절염 자가줄기세포 치료제인 조인트스템의 국내외 임상 2상 결과를 발표했다. 미국 환자 26명을 대상으로 한 임상에서 효과를 입증했다는 것이다.
네이처셀은 이 같은 결과를 바탕으로 지난 6월 식품의약품안전처에 조건부 허가를 신청했고 이달 허가를 받고 시판할 계획이었다. 네이처셀 관계자는 "식약처 심사 과정에서 허가가 지연되고 있다"며 "연내 시판은 어려울 것"이라고 말했다.
조인트스템은 자가줄기세포를 활용한 중증 퇴행성 관절염 치료제다. 인공관절 수술 없이 1회 주사로 효과가 있고 자신의 세포를 활용해 면역거부반응이 없다는 게 회사 측 설명이다.
조인트스템의 미국 임상을 담당한 세다스시나이메디컬센터의 티머시 데이비스 정형외과 전문의는 “중증 관절염 환자 26명을 대상으로 6개월간 추적 연구한 결과 조인트스템이 통증을 줄여주고 관절의 뻣뻣함을 개선했다”고 말했다.
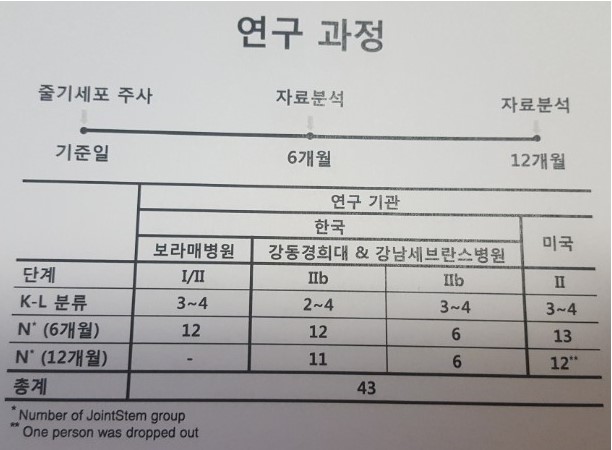
네이처셀은 보라매병원과 강동경희대병원, 강남세브란스병원 등 세 곳에서 독자적으로 조인트스템의 국내 임상 2상을 했다. 미국에서 추가로 한 임상 건수까지 합치면 44건이다.
퇴행성 관절염 치료제 중 제대혈 유래 줄기세포를 이용한 메디포스트의 카티스템은 국내 병원 10곳에서 103명의 환자를 대상으로 임상 3상을 했고 코오롱생명과학의 유전자치료제 인보사는 국내 병원 12곳에서 159명을 대상으로 한 임상 3상 결과를 식약처에 제출했다. 경쟁 제품과 비교해 통계적으로 효능을 입증할 자료가 부족하다는 지적이 나오는 이유다.
네이처셀은 문제가 없다는 입장이다. 라정찬 바이오스타줄기세포기술연구원장은 “환자마다 맞춤형 치료제를 개발했고 투여한 환자의 90% 이상이 호전됐기 때문에 의미가 있다”고 설명했다. 이어 “인보사가 생리식염수와 효과를 비교한 것과 달리 조인트스템은 미국 식품의약국(FDA) 허가를 받은 히알루론산 제품을 대조약으로 사용했다”며 “식약처의 조건부 허가 기준을 만족한다”고 주장했다.
네이처셀은 6월 조건부 허가 신청 이후 두 차례 설명회를 열어 조인트스템 홍보에 나섰다. 네이처셀 주가는 한 달간 두 배 이상 급등했다. 업계 관계자는 “논문이나 학회 발표 등 과학적인 데이터를 통해 임상 결과를 인정받아야 한다”고 말했다.
전예진 기자 ace@hankyung.com
기업의 환율관리 필수 아이템! 실시간 환율/금융서비스 한경Money
[ 무료 주식 카톡방 ] 국내 최초, 카톡방 신청자수 35만명 돌파 < 업계 최대 카톡방 > --> 카톡방 입장하기!!
관련뉴스














