지난 주요뉴스 한국경제TV에서 선정한 지난 주요뉴스 뉴스썸 한국경제TV 웹사이트에서 접속자들이 많이 본 뉴스 한국경제TV 기사만 onoff
-
GC녹십자, 세계심포지엄서 리소좀축적질환 치료제 개발 동향 발표 2024-02-13 09:31:44
단계에서 증명된 효능과 안전성을 바탕으로 미국 FDA와 유럽 EMA로부터 희귀의약품 (ODD) 지정을 받은 바 있다. 이번 심포지엄에서 MPS IIIA 질환마우스에서 증명된 우수한 헤파란 황산염(Heparan sulfate) 감소 효과와 뇌병변 개선 결과를 발표했다. 파브리병은 알파-갈락토시다아제의 결핍으로 당지질이 축적돼 주로...
- 뉴스 > 산업
- 바로가기

-
셀트리온, 악템라 바이오시밀러 'CT-P47' 유럽 품목허가 신청 2024-02-13 09:29:03
셀트리온은 유럽의약품청(EMA)에 자가면역질환 치료제 '악템라(Actemra, 성분명 : 토실리주맙)' 바이오시밀러 'CT-P47'의 품목허가 신청을 완료했다고 13일 밝혔다. 셀트리온은 류마티스 관절염(RA), 거대세포동맥염(GCA), 전신형 소아 특발성 관절염(sJIA), 다관절형 소아 특발성 관절염(pJIA),...
- 뉴스 > 산업
- 바로가기

-
셀트리온, 류머티즘약 '악템라' 바이오시밀러 유럽 허가 신청 2024-02-13 09:11:36
의약품청(EMA)에 자가면역질환 치료제 '악템라'(성분명 토실리주맙)의 바이오시밀러(바이오의약품 복제약)인 'CT-P47'의 품목허가를 신청했다고 13일 밝혔다. 류머티즘 관절염, 거대세포동맥염, 전신형 소아 특발성 관절염, 코로나19 등 유럽에서 악템라를 사용하는 전체 치료 범위(적응증)에 대해 신청이...
- 뉴스 > 경제
- 바로가기

-
경쟁사 J&J 임상 성공에도 한올바이오파마가 웃는 이유 2024-02-10 21:08:10
유럽 의약품청(EMA) 허가신청 일정을 알릴 것으로 예상했다. 그는 "우리나라에서 개발된 신약이면서 동종 계열 약물 중 가장 최고로 손꼽히는 약물이 올해 임상 3상을 마무리하고 승인 신청될 것"이라며 "한올바이오파마가 미국과 유럽에서 발생한 매출에 따라 로열티를 수령하게 된다는 의미"라고 했다. 실제 박승국...
- 뉴스 > IT·과학
- 바로가기

-
'비만치료 ETF' 나온다…14일 신규 상장 2024-02-08 11:46:55
또는 유럽의약품청(EMA)에 승인된 비만치료제 또는 체중 감소 기능 의약품이 있거나 임상시험이 진행 중인 기업 중 선정한다. 1좌당 가격은 1만원이다. ETF 상품은 운용비용이나 구성 종목 교체 등에 따라 지수 성과와 운용성과 간 괴리가 발생할 수 있으며, 환노출 ETF의 경우 향후 환율 변동위험에 노출될 수 있다는...
- 뉴스 > 증권
- 바로가기

-
국내 첫 '비만치료 ETF' 나온다…14일 상장 2024-02-08 11:32:45
종목 선정은 미국 식품의약청(FDA) 또는 유럽의약품청(EMA)에 승인된 비만치료제 또는 체중 감소 기능 의약품이 있거나 임상시험이 진행 중인 기업 중 선정한다. 1좌당 가격은 1만원이다. ETF 상품은 운용비용이나 구성 종목 교체 등에 따라 지수 성과와 운용성과 간 괴리가 발생할 수 있다. 또 환노출 ETF의 경우 향후 ...
- 뉴스 > 경제
- 바로가기

-
에이프로젠, 항암제 '허셉틴' 복제약 3상 계획 인도서 승인 2024-02-05 08:10:51
위한 임상3상을 하겠다고 유럽의약품청(EMA)에 신청했다. 이어 11월에는 인도 중앙의약품표준국(CDSCO)에도 같은 내용으로 임상3상 신청을 했다. 에이프로젠은 "3상 임상시험 완료 후에는 유럽 이외 인도뿐만 아니라 미국 FDA(식품의약청) 및 다른 국가에 품목허가신청을 계획하고 있다"고 밝혔다. rao@yna.co.kr (끝)...
- 뉴스 > 경제
- 바로가기

-
BMS‘아베크마’ 유럽서 다발성골수종 3차치료제 승인 권고 2024-01-29 14:46:01
여부를 결정할 예정이다. 지난 26일(현지시간) BMS는 유럽의약품청(EMA) 인체의약품위원회(CHMP)가 아베크마를 재발성 또는 불응성 다발성 골수종 성인 환자의 3차 치료제로 승인할 것을 권고했다고 밝혔다. 아베크마는 BCMA를 표적하는 키메릭항원수용체-T(CAR-T)세포치료제다. CHMP는 아베크마의 임상 3상 ‘KarMMa-3’...
- 뉴스 > IT·과학
- 바로가기
-
대웅제약, '베르시포로신' 유럽 희귀의약품 지정 2024-01-29 09:49:13
있도록 지원하는 제도다. EMA는 유럽에서 인구 1만명 중 5명 이하로 영향을 주는 질병 중 미충족 의료 수요가 높고 환자들에게 상당한 혜택(Significant Benefit)이 예상되는 후보물질을 희귀의약품으로 지정하고 있다. EMA의 희귀의약품 지정을 받은 후보물질은 ▲임상시험에 대한 과학적 조언 제공 ▲허가 수수료 감면...
- 뉴스 > 산업
- 바로가기
-
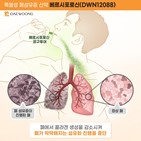
대웅제약 "특발성 폐섬유증 신약, 유럽서 희귀의약품 지정" 2024-01-29 09:46:02
유럽 의약품청(EMA)으로부터 희귀의약품으로 지정받았다고 29일 밝혔다. 이 제도는 희귀난치성 질환 치료제의 개발과 허가가 원활히 이뤄질 수 있도록 지정된 후보물질에 대해 임상시험 조언, 허가 수수료 감면, 허가 시 10년간 독점권 인정 등 혜택을 부여하는 제도다. 특발성 폐섬유증은 폐에 콜라겐이 과도하게 축적돼...
- 뉴스 > 경제
- 바로가기