지난 주요뉴스 한국경제TV에서 선정한 지난 주요뉴스 뉴스썸 한국경제TV 웹사이트에서 접속자들이 많이 본 뉴스 한국경제TV 기사만 onoff
-
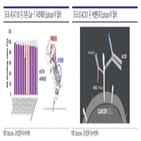
“앱클론, 3분기 CAR-T 및 항체 치료제 긍정적 결과 발표 기대“ 2022-08-30 08:13:41
전체 투약군 ORR은 77.3%, 일부 공개된 저용량 투약군의 ORR은 100%였다. 이 효능 데이터를 바탕으로 추정한 예상치다. 현재 위암 1차 치료의 표준치료법(SoC)은 기존 ‘허셉틴’ 치료의 ORR 40~50%을 능가한 ‘키트루다’와 허셉틴 병용이다. 이들 병용 치료의 ORR은 74%다. 헨리우스는 10월 2상 결과를 공개하고, 내년...
- 뉴스 > IT·과학
- 바로가기
-
오스코텍, 1200억원 주주배정 유증…"선제적 투자 일환" 2022-08-29 09:55:49
반응이 없었다고 가정하면 투약군의 반응률은 40% 이상이며, 고용량군의 반응률은 더 높았을 것으로 기대 중이다. 세비도플레닙이 오스코텍의 두번째 글로벌 신약이 될 것으로 예상하고 있다. 오스코텍은 세비도플레닙의 적응증 확장을 위해 복수의 자가면역질환을 대상으로 추가적인 임상을 계획 중이다. SKI-G-801은...
- 뉴스 > IT·과학
- 바로가기
-
“메디포스트, 대주주 변경으로 사업개편 및 빠른 임상 기대” 2022-08-29 09:03:29
사업군의 매출 비중은 제대혈보관 49%, 세포치료제 카티스템 30%, 건강기능식품 21%다. 매출은 600억원에 근접하지만 최근 영업적자는 확대되고 있다. 고비용 구조를 개선하고 임상 및 연구개발비의 변수를 조절하는 등 영업흑자가 발생하는 구조로 변화를 꾀할 수 있다는 판단이다. 자금력 강화하며 빠른 임상 기대임상은...
- 뉴스 > IT·과학
- 바로가기

-
뉴지랩파마 “국내 폐암치료 임상2상서 부분관해율 75%” 2022-08-24 17:56:55
치료군’을 대상으로 한 시험에서 확인된 사례다. 탈레트렉티닙은 지난 6월 국내 식품의약품안전처로부터 임상시험 대상을 기존 2차 치료제 투약군에 이어 1차 치료제 투약군으로 확대해, 1, 2차 치료제로 변경 승인을 받은 바 있다. 미국 안허트테라퓨틱스가 올해 미국임상종양학회(ASCO)에서 발표한 글로벌 임상 2상...
- 뉴스 > 산업
- 바로가기

-
뉴지랩테라퓨틱스, 폐암 치료제 2상서 부분관해율 75% 확인 2022-08-24 13:46:43
치료제 투약군에 이어 1차 치료제 투약군으로 확대해, 1·2차 치료제로 변경 승인 받았다. 향후 진행될 1차 치료제 투약군 대상 임상에서 더욱 증대된 효능을 보일 것으로 기대하고 있다. 탈레트렉티닙은 글로벌 임상에서도 1차 치료군에서 완전관해 2건을 확인하는 등 치료효과를 확인했다. 미국 안허트테라퓨틱스는 올해...
- 뉴스 > IT·과학
- 바로가기
-
애스톤사이언스, 암 치료 백신 ‘AST-301’ 美 2상 승인 2022-08-24 08:55:52
군 무작위 배정 설계(디자인)를 적용했다. HER2 저발현 유방암 수술 후 재발 가능성이 높은 환자들을 대상으로 표준 치료제인 ‘젤로다’ 또는 ‘키트루다’와 병용 투약한다. 이번 2상은 3상과 동일한 환자군과 디자인이 적용됐다고 회사는 전했다. 중간 결과에 따라 신속 허가(BLA)에 대한 논의나 확증적 임상 자료를...
- 뉴스 > IT·과학
- 바로가기
-
셀트리온 "유럽서 휴미라 시밀러-오리지널약 '상호교환' 임상" 2022-08-23 10:45:36
휴미라를 여러 차례 교차해 투약한 환자군과 휴미라만 투약한 환자군 등 두 집단 사이의 약물의 유효성과 안전성 등을 비교·검증하는 방식이다. 유플라이마가 휴미라와의 상호교환성을 인정받으면 의사의 개입 없이 약국에서 대체 처방 등이 가능해지고, 휴미라를 투약하던 환자들도 치료 도중에 유플라이마를 처방받는...
- 뉴스 > 경제
- 바로가기
-
셀트리온, 휴미라 바이오시밀러 교차처방 유럽 임상 3상 신청 2022-08-23 10:33:38
간 다회 교차 투약군과 휴미라 유지 투약군 간의 약동학 유효성 안전성 등을 비교한다. 셀트리온은 앞서 류머티즘 관절염 환자를 대상으로 한 유플라이마 글로벌 3상을 통해 휴미라와 유사한 유효성 및 약동학, 안전성 결과를 확인했다. 이를 통해 2021년 2월 휴미라가 보유한 모든 적응증에 대해 유플라이마의 유럽...
- 뉴스 > IT·과학
- 바로가기
-
널뛰기 한 헬릭스미스 주가…기다렸던 'IDMC 권고' 뭐였길래 [한재영의 바이오 핫앤드콜드] 2022-08-20 11:45:44
이상 여부 검수를 위해 취한 조치들에 대한 요약 리뷰를 검토하였다. 현재 위약군과 투약군 간의 차이를 증명할 수 있는 최소 숫자인 152명에 대한 등록이 거의 완료되었고, DSMB(Data Safety Monitoring Board) 리포트에 따르면 그룹 간의 이상 반응(Adverse Event)에서 차이가 없으므로, IDMC는 헬릭스미스에게 계획대로...
- 뉴스 > IT·과학
- 바로가기

-
헬릭스미스 "IDMC, DPN 3-2상 추가 중간분석 실시 권고" 2022-08-18 15:57:49
때 투약군과 위약군 간 이상반응에서 차이가 없어 엔젠시스가 안전하다고 판단했다. 또 현재 152명에 대한 등록이 거의 완료된 점을 감안해, 기등록된 환자들에 대해 추가 중간분석을 실시해 임상 진행 여부를 결정할 것을 권고했다. 회사 측은 "권고에서는 언급되지 않았지만, 계획된 통계 분석 대상자 76명 중 실제 분석...
- 뉴스 > IT·과학
- 바로가기





