지난 주요뉴스 한국경제TV에서 선정한 지난 주요뉴스 뉴스썸 한국경제TV 웹사이트에서 접속자들이 많이 본 뉴스 한국경제TV 기사만 onoff
-
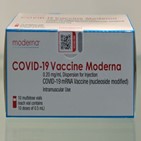
식약처, 내일 모더나 백신 검증결과 발표…사용승인 받을까 2021-05-09 11:43:37
식품의약품안전처가 모더나의 신종 코로나바이러스 감염증(코로나19) 예방백신 검증결과에 대해 발표할 예정이다. 9일 식약처에 따르면 검증자문단은 이날 회의를 진행하고, 10일 결과를 발표할 예정이다. 검증자문단은 감염내과 교수 등 백신 관련 전문가로 구성됐으며, 모더나 코로나19 백신의 임상·비임상 품질 분야에...
- 뉴스 > 생활문화
- 바로가기
-
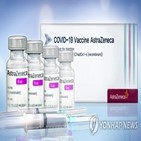
"아스트라제네카, 미국에 코로나 백신 정식승인 요청 검토" 2021-05-08 09:41:14
의약품 활용도를 높이기 위해 내리는 임시 조치다. 반면 정식 승인 절차는 요건이 엄격하며 수개월이 소요되는 것으로 알려져 있다. 아스트라제네카가 정식 승인 신청을 검토하는 것은 긴급사용 승인 신청이 지연되고 있기 때문이라고 WSJ은 전했다. 앞서 아스트라제네카는 지난달 중순까지 긴급사용 승인을 신청하겠다고...
- 뉴스 > 정치·사회·국제
- 바로가기
-
유럽의약품청, AZ 백신 접종 후 길랭-바레 증후군 보고사례 검토 2021-05-08 02:26:05
유럽의약품청, AZ 백신 접종 후 길랭-바레 증후군 보고사례 검토 (브뤼셀=연합뉴스) 김정은 특파원 = 유럽의약품청(EMA)은 7일(현지시간) 다국적 제약사 아스트라제네카(AZ) 신종 코로나바이러스 감염증(코로나19) 백신 접종 후 보고된 길랭-바레 증후군(GBS·Guillain-Barre Syndrome) 사례에 대한 자료를 분석하고 있다고...
- 뉴스 > 정치·사회·국제
- 바로가기

-
화이자, 美 FDA에 백신 '정식 승인' 요청…승인 시 직접 판매 가능 2021-05-07 23:43:37
자료 등을 제출했다. 앞서 화이자는 지난해 12월 FDA로부터 코로나19 백신의 긴급사용을 승인받았다. '긴급사용 승인'은 공중보건 위기가 닥쳤을 때 의약품의 활용도를 높이기 위해 내리는 일시적 조치로 정식 절차보다 승인 요건이 비교적 엄격하지 않다. FDA에 코로나19 백신에 대한 '정식 승인'을...
- 뉴스 > 생활문화
- 바로가기

-
화이자, 미 FDA에 코로나19 백신 정식 승인 요청 2021-05-07 23:18:00
자료 등을 제출했다고 보도했다. FDA에 코로나19 백신에 대한 정식 승인을 요청한 것은 화이자가 최초다. 화이자는 지난해 12월 FDA로부터 긴급사용을 승인받았다. 긴급사용 승인은 공중보건 위기가 닥쳤을 때 의약품의 활용도를 높이기 위해 내리는 일시적 조치로 정식 절차보다 승인 요건이 상대적으로 엄격하지 않다....
- 뉴스 > 정치·사회·국제
- 바로가기

-
화이자, 미국 FDA에 코로나19 백신 정식 승인 요청 2021-05-07 23:10:32
자료 등을 제출했다고 보도했다. FDA에 코로나19 백신에 대한 정식 승인을 요청한 것은 화이자가 최초다. 화이자는 지난해 12월 FDA로부터 긴급사용을 승인받았다. 긴급사용 승인은 공중보건 위기가 닥쳤을 때 의약품의 활용도를 높이기 위해 내리는 일시적 조치로 정식 절차보다 승인 요건이 상대적으로 엄격하지 않다....
- 뉴스 > 정치·사회·국제
- 바로가기

-
EMA "화이자·바이오엔테크 백신 12세 이상에 사용허용 검토" 2021-05-04 07:21:48
유럽의약품청(EMA)이 화이자·바이오엔테크의 신종코로나바이러스 감염증(코로나19) 백신 사용을 12세 이상에 대해 허용할지 여부를 검토한다. 3일(현지시간) DPA통신에 따르면 EMA는 "화이자·바이오엔테크가 제출한 자료에 대해 빠르게 검토를 거쳐 다음달 결과를 발표할 것"이라고 밝혔다. 다만 추가 자료가 필요할 경우...
- 뉴스 > 정치·사회·국제
- 바로가기
-
EMA "화이자 백신 12세 이상에 사용허용 검토…내달 결론" 2021-05-04 02:03:24
의약품청(EMA)이 화이자·바이오엔테크의 신종코로나바이러스 감염증(코로나19) 백신 사용을 12세 이상에 대해 허용할지 검토에 착수했다. EMA는 3일(현지시간) "화이자·바이오엔테크가 제출한 자료에 대해 빠르게 검토를 거쳐 다음달 결과를 발표할 것"이라고 밝혔다고 DPA통신이 전했다. 다만, 추가 자료가 필요할 경우...
- 뉴스 > 정치·사회·국제
- 바로가기

-
셀트리온, 코로나19 자가검사키트 식약처 조건부 허가 2021-05-03 09:12:25
셀트리온제약을 포함한 여러 유통망을 통해 공급할 계획이다. 셀트리온은 지난 2월과 3월 미국에서 소아 및 성인 포함 약 450여명을 대상으로 진행한 임상시험 결과를 미국 식품의약국(FDA)에 제출했으며 현재 심사결과를 기다리고 있다. 셀트리온은 이번 조건부 허가에 따라 식약처에 자가검사키트에 대한 추가...
- 뉴스 > 산업
- 바로가기

-
지난해 신약 40개 품목허가…국내 개발 신약은 '0개' 2021-05-03 09:00:02
희귀의약품 품목허가 건수는 2016년 34개에서 2019년 11개로 감소하다가 지난해에는 상승세로 돌아서 24개(14개 성분)가 허가됐다. 기존 의약품의 성분을 섞거나 일부 염을 바꾸는 등의 방식으로 개발돼 안전성·유효성 심사 자료를 제출해야 하는 '자료제출의약품' 326개 중에서는 '새로운 조성 제품'이...
- 뉴스 > 경제
- 바로가기






