지난 주요뉴스 한국경제TV에서 선정한 지난 주요뉴스 뉴스썸 한국경제TV 웹사이트에서 접속자들이 많이 본 뉴스 한국경제TV 기사만 onoff
-
제넥신 "합병 통해 항암제 파이프라인 신규 개발"[KIW2024] 2024-09-11 13:36:09
"현재 개발중인 후보물질 EPD-301의 경우 내년까지 임상시험 계획(IND) 승인 완료를 목표로 하고 있다"며 "국내 임상 1상 진입과 함께 2026년까지는 글로벌 회사로의 기술이전을 추진할 예정"이라고 말했다. 그는 "해당 파이프라인은 IND 단계가 됐을 때 기술이전 계약을 할 의사가 있는 글로벌 사가 다수 존재하기 때문에...
- 뉴스 > IT·과학
- 바로가기

-
대웅제약, 서울대와 손잡고 내성 극복 독감 치료제 개발 추진 2024-09-11 09:25:29
및 임상약 생산·허가를, 대웅바이오는 원료 합성법 개발 및 GMP(의약품 제조·품질관리기준) 생산, 서울대는 물질 개발, 한국화학연구원은 생체 외(in vitro), 생체 내(In vivo) 효력 및 독성시험을 담당한다. 이번 연구의 목표는 '타미플루'로 알려진 항바이러스제 성분 '오셀타미비르'의 내성 문제를...
- 뉴스 > 경제
- 바로가기

-
한독 "관계사 고인슐린증 치료제, 美 임상 보류 조치 해제" 2024-09-10 16:35:54
한독에 따르면 FDA는 RZ358에 대한 동물 시험에서 간 독성 문제가 확인됐다며 미국에서의 임상 3상 진행을 보류한 바 있다. FDA는 해당 문제가 특정 동물 종에 국한되는 문제로, 사람과는 관련성이 없다고 결론 내렸다고 레졸루트가 전했다. RZ358은 인슐린 수용체 특정 부위에 작용하는 단일클론항체로, 레졸루트가 유럽...
- 뉴스 > 경제
- 바로가기

-
삼성에피스·셀트리온, '키트루다' 바이오시밀러 개발 속도 낸다 2024-09-10 16:01:27
말 유럽의약품청(EMA)에 키트루다 바이오시밀러 ‘CT-P51’ 임상 3상 시험계획서를 제출했다. 오리지널 약물이 승인받은 모든 적응증에 대해 허가 승인을 받고 시장 및 매출 확대를 노릴 계획이다. 키트루다의 물질특허는 한국과 미국, 유럽에서 각각 2028년 6월, 2029년 11월, 2031년 1월에 만료된다. 셀트리온은 6월 미국...
- 뉴스 > IT·과학
- 바로가기

-
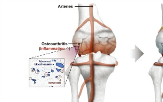
노인 여성 절반 앓는 '관절염'…넥스트바이오, 새로운 통증 완화법 내놔 2024-09-10 16:00:57
제품의 임상시험계획 승인을 획득했다고 지난 6일 밝혔다. 넥스피어 에프의 성분은 생분해되고 효과가 빠르게 나타나는(속효성) 미립구로, 통증을 유발하는 신경세포를 괴사시킨 뒤 2~6시간 이내에 분해된다. 분해되지 않는 다른 제품에 비해 피부 변색과 괴사 등의 부작용을 극복했다는 평도 받는다. 특히 회사는 일본에서...
- 뉴스 > IT·과학
- 바로가기
-
지씨셀, 이뮨셀엘씨주 인도네시아 비파마에 기술이전 2024-09-10 15:08:32
항암면역세포치료제다. 환자의 혈액에서 면역세포를 분리해 2~3주간 세포 배양을 거쳐 살해세포의 암세포 사멸 기능을 크게 향상시킨 자가혈액유래 T 림프구를 주성분으로 한다. 초기 간세포암종 환자 대상 3상 임상시험에서 대조군 대비 재발 위험을 37% 낮추고 사망률을 79% 낮추는 효과를 입증해 간암 수술 후 치료제로...
- 뉴스 > IT·과학
- 바로가기

-
대웅제약, 마이크로니들 패치 성장호르몬제 임상시험계획 승인 2024-09-10 10:58:04
패치 성장호르몬제 임상시험계획 승인 "주사제 비해 통증 없이 맞을 수 있어 환자 편의성 개선" 비만치료제 등으로 마이크로니들 패치 확대 계획 (서울=연합뉴스) 나확진 기자 = 대웅제약[069620]이 기존 주사제에 비해 투여 시 통증이 거의 없는 마이크로니들 패치(미세한 침을 반창고처럼 붙이는 제제) 형태의 성장호르몬...
- 뉴스 > 경제
- 바로가기

-
코오롱제약, 에스트리온과 삼중음성유방암 신약 공동개발 2024-09-10 09:51:51
전임상시험을 공동 수행할 계획이다. 에스트리온은 저분자 합성의약품 개발 경험과 노하우를 바탕으로 시료 생산부터 GLP 독성시험 등 비임상시험을 수행하고 사업개발에도 참여한다. 삼중음성유방암은 에스트로겐 수용체(ER), 프로게스테론 수용체(PR), 인간표피성장인자 수용체 2형(HER2)이 모두 음성인 유방암이다. 암...
- 뉴스 > IT·과학
- 바로가기

-
신약 허가 수수료 883만원→4억1천만원 대폭 인상(종합) 2024-09-09 18:54:20
운영해 업계에 허가 단계별 전문 상담을 제공하고, 임상 시험과 제조·품질관리기준(GMP)은 우선 심사할 계획이다. 또 규제 역량 강화를 위해 전문 의사·약사 등 전문 심사자 비율을 기존 31%에서 70% 이상으로 높이고, 규제 지원을 위한 맞춤형 상담 대면 회의를 기존 3회에서 10회 이상으로 확대하는 내용도 포함됐다....
- 뉴스 > 경제
- 바로가기

-
"신약 허가 수수료 800만원→4억으로 인상…인력 늘려 심사기간 단축" 2024-09-09 18:29:04
있다”며 “개정안이 안착되면 임상시험계획(IND) 심사 기간을 단축하는 등 확대 방안도 검토 중”이라고 말했다. 수수료를 올리더라도 심사 수준을 높여달라는 것은 업계의 오랜 요구사항이었다. FDA는 건당 50억원에 달하는 심사 수수료를 받는 대신 어떻게 임상전략을 짜야 할지 꼼꼼히 코칭해준다. 수십억원의 수수료로...
- 뉴스 > IT·과학
- 바로가기






